Diversidade microbiana no ambiente e em partes do trono imperial de D. Pedro II - caracterização por microbiologia clássica e biologia molecular antes e após intervenções de conservação e restauro
DOI:
https://doi.org/10.14568/cp2019020Palavras-chave:
Trono de D. Pedro II, Bactérias, Fungos, Biologia Molecular, Diversidade MicrobianaResumo
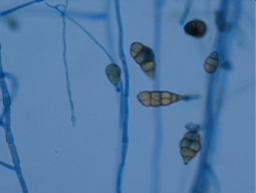
O Museu Imperial tem uma importante coleção histórica da Família Real Portuguesa no Brasil. O trono representa o poder imperial, e é considerado uma das peças mais importantes do Museu. Entretanto, vinha enfrentando há décadas uma deterioração gradual, principalmente devido aos seus componentes em tecido. Devido ao interesse em preservar o objeto, processos de conservação e restauro foram executados em todas as partes do trono. Como parte deste tratamento, uma inspeção microbiológica foi executada em partes selecionadas do objeto, bem como no seu ambiente de guarda. Este estudo de biodeterioração, controle e detecção de espécies microbianas indicou uma clara resposta em relação ao local de guarda, e então o processo de restauro pode ser executado visando solucionar os danos mais pronunciados objetivando restaurar as características originais do artefacto. O estudo indicou uma alta diversidade de fungos e bactérias. Foi observada uma redução de espécies fúngicas detectadas no trono antes e após o restauro, observando-se a recorrência dos gêneros Absidia, Cladosporium e Epicoccum. Essa redução não foi muito pronunciada para as bactérias, observando-se, também, recorrência bacteriana após o restauro (Microbacterium, Staphylococcus e Kocuria). No ar, observou-se o aparecimento de novas espécies fúngicas após o restauro, indicando recontaminação natural na área expositiva.
Downloads
Referências
[1] Zanatta, E. M., ‘Subjetividade e objetividade: as decisões nos processos de conservação e restauração dos bens culturais’, Tese de Doutoramento, Universidade do Federal do Estado do Rio de Janeiro/UNIRIO e Museu de Astronomia e Ciências Afins/MAST, Rio de Janeiro (2017).
[2] Pasquarella, C.; Balocco, C.; Pasquariello, G.; Petrone, G.; Saccani, E.; Manotti, P.; Ugolotti. M.; Palla, F.; Maggi, O.; Albertini, R., ‘A multidisciplinary approach to the study of cultural heritage environments: Experience at the Palatina Library in Parma’, Science of the Total Environment 536 (2015) 557-567, https://doi.org/10.1016/j.scitotenv.2015.07.105.
[3] Wenzel, M.; Schönig, I.; Berchtold, M.; Kämpfer, P.; König, H., ‘Aerobic and facultatively anaerobic cellulolytic bacteria from the gut of the termite Zootermopsis angusticollis’, Journal of Applied Microbiology 92(1) (2002) 32-40, https://doi.org/10.1046/j.1365-2672.2002.01502.x.
[4] Di Carlo, E.; Chisesi, R.; Barresi, G.; Barbaro, S.; Lombardo, G.; Rotolo, V.; Sebastianelli, M.; Travagliato, G.; Palla, F., ‘Fungi and bacteria in indoor cultural heritage environments: microbial-related risks for artworks and human health’, Environment and Ecology Research 4(5) (2016) 257-264, https://doi.org/10.13189/eer.2016.040504.
[5] Sterflinger, K.; Piñar, G., Microbial deterioration of cultural heritage and works of art – tilting at windmills?’, Applied Microbiology and Biotechnology 97 (2013) 9637-9646, https://doi.org/10.1007/s00253-013-5283-1.
[6] Akinyale, H. A., ‘Isolation of bacteria with potential for production of thermostable extracellular cellulase from sawdust’, Tese (Doutorado), Faculty of Science, University of Ibadan (2014).
[7] Gerber, E.; Bernard, R.; Castang, S.; Chabot, N.; Coze, F.; Dreux-Zigha, A.; Hauser, E.; Hivin, P.; Joseph, P.; Lazarelli, C.; Letellier, G.; Olive, J.; Leonetti, J. P., ‘Deinococcus as new chassis for industrial biotechnology: biology, physiology and tools’, Journal of Applied Microbiology 119(1) (2015) 1-10, https://doi. org/10.1111/jam.12808.
[8] Li, Q.; Zhang, B.; Yang, X.; Ge, Q., ‘Deterioration-associated microbiome of stone monuments: structure, variation, and assembly’, Applied Environmental Microbiology 84(7) (2018) 2680-2687, https://doi.org/10.1128/AEM.02680-17.
[9] Johnson, T. A.; Sims, G. K.; Ellsworth, T. R.; Ballance, A. R., ‘Effects of moisture and sorption on bioavailability of p-hydroxybenzoic acid to Arthrobacter sp. in soil’, Microbiological Research 153(4) (1999) 349-353, https://doi.org/10.1016/S0944-5013(99)80049-4.
[10] Mongodin, E. F.; Shapir, N.; Daugherty, S. C.; Deboy, R. T.; Emerson, J. B.; Shvartzbeyn, A.; Radune, D.; Vamathevan, J.; Riggs, F.; Grinberg, V.;Khouri, H.; Wackett, L. P.; Nelson, K. E.; Sadowsky, M. J., ‘Secrets of soil survival revealed by the genome sequence of Arthrobacter aurescens TC1’, PLoS Genetics 2(12) (2006) 2094-2106, https://doi.org/10.1371/journal.pgen.0020214.
[11] Marvasi, M.; Vedovato, E.; Balsamo, C.; Macherelli, A.; Dei, L.; Mastromei, G.; Perito, B., ‘Bacterial community analysis on the Mediaeval stained glass window “Natività” in the Florence Cathedral’, Journal of Cultural Heritage 10(1) (2009) 124-133, https://doi.org/10.1016/j.culher.2008.08.010.
[12] Suihko, M. L.; Alakomi, H. L.; Gorbushina, A.; Fortune, I.; Marquardt, J.; Saarela, M., ‘Characterization of aerobic bacterial and fungal microbiota on surfaces of historic Scottish monuments’, Systematic and Applied Microbiology 30(6) (2007) 494-508, https://doi.org/10.1016/j.syapm.2007.05.001.
[13] Gutarowska, B.; Skora, J.; Zduniak, K.; Rembisz, D., ‘Analysis of the sensitivity of microorganisms contaminating museums and archives to silver nanoparticles’, International Biodeterioration & Biodegradation 68 (2012) 7-17, https://doi.org/10.1016/j.ibiod.2011.12.002.
[14] Saarela, M.; Alakomi, H. L.; Suihko, M. L.; Maunuksela, L.; Raaska, L.; Mattila- Sandholm, T., ‘Heterotrophic microorganisms in air and biofilm samples from Roman catacombs, with special emphasis on actinobacteria and fungi’, International Biodeterioration & Biodegradation 54(1) (2004) 27-37, https://doi.org/10.1016/j.ibiod.2003.12.003.
[15] Wang, W.; Ma, Y.; Ma, X.; Wu, F.; Ma, X.; An, L.; Feng, H., ‘Diversity and seasonal dynamics of airborne bacteria in the Mogao Grottoes, Dunhuang, China’, Aerobiologia 28(1) (2012) 27-38, https://doi.org/10.1007/s10453-011-9208-0.
[16] Heyrman, J.; Swings, J., ‘16S rDNA Sequence analysis of bacterial isolates from biodeteriorated mural paintings in the Servilia Tomb (Necropolis of Carmona, Seville, Spain)’, Systematic and Applied Microbiology 24(3) (2001) 417-422, https://doi.org/10.1078/0723-2020-00048.
[17] Lutterbach, M. T. S.; Oliveira, A.L.C.; Zanatta, E.; da Costa, A. C. A., ‘A berlinda de aparato do imperador D. Pedro II: identificação de fungos em partes selecionadas e sua relação com biodeterioração e aerobiologia’, Conservar Património 17 (2013) 59- 72, https://doi.org/10.14568/cp2013003.
[18] da Costa, A. C. A.; Corrêa, F. N.; Lino, L. A. S.; Almeida, E. H. P.; Oliveira, A. L. C.; Lutterbach, M. T. S., 'Microbiological characterization of contaminating cells on scientific collections in a specialized library', Annual Research & Review in Biology 4 (2014) 3915-3931, https://doi.org/10.9734/ARRB/2014/11395.
[19] Kim, M. J.; Shin, H. K.; Choi, Y. S.; Kim, G. C.; Kim, G. H., ‘An aeromycological study of various wooden cultural heritages in Korea’, Journal of Cultural Heritage 17 (2016) 123-130, https://doi.org/10.1016/j.culher.2015.05.001.
[20] Coutinho, M. L.; Miller, A. Z.; Macedo, M. F., 'Biological colonization and biodeterioration of architectural ceramic materials: An overview', Journal of Cultural Heritage 16 (2015) 759-777, https://doi.org/10.1016/j.culher.2015.01.006.
[21] Ruga, L.; Orlandi, F.; Romano, B.; Fornaciari, M. ‘The assessment of fungal bioaerosols in the crypt of St. Peter in Perugia (Italy)’, International Biodeterioration & Biodegradation 98 (2015) 121-130, https://doi.org/10.1016/j.ibiod.2014.12.010.
[22] Do Campo, S.; Trigo, M. M.; Recio, M.; Melgar, M.; García-Sanchez, J.; Cabezudo, B., 'Fungal spore content of the atmosphere of the Cave of Nerja (southern Spain): diversity and origin', Science of the Total Environment 409 (2011) 835-843, https://doi.org/10.1016/j.scitotenv.2010.10.048.
[23] Porca, E.; Jurado, V.; Martin-Sanchez, P. M.; Hermosín, B.; Bastian, F.; Alabouvette, C.; Sáiz-Jiménez, C., ‘Aerobiology: an ecological indicator for early detection and control of fungal outbreaks in caves’, Ecological Indicators 11(6) (2011) 1594-1598, https://doi.org/10.1016/j.ecolind.2011.04.003.
[24] Martin-Sanchez, P. M.; Bastian, F.; Alabouvette, C.; Saiz- Jimenez, C., ‘Real-time PCR detection of Ochroconis lascauxensis involved in the formation of black stains in the Lascaux Cave, France’, Science of the Total Environment 443 (2013) 478-484, https://doi.org/10.1016/j.scitotenv.2012.11.026.
Downloads
Publicado
Como Citar
Edição
Secção
Licença
O presente trabalho é distribuído nos termos da Licença Creative Commons (CC BY-NC 4.0) que permite a utilização, partilha e reprodução para fins não comerciais e sem modificações, desde que o autor e fonte original sejam citados.
O Copyright permanece com os autores.